
- 00Días
- 00Horas
- 00Minutos
- 00Segundos

El ácido láctico es un ingrediente que ha sido muy utilizado en cosmética natural, tanto por sus características ácidas, para ajustar el pH final de las formulaciones cosméticas, como por sus propiedades exfoliantes e hidratantes únicas. En el mercado podemos encontrarlo en la forma ácida, que hace que esté considerado dentro del grupo de los alfa hidroxiácidos, y en forma de sal, formando parte de los componentes del Factor de Hidratación Natural de la piel (NMF).
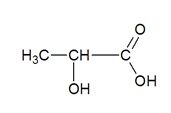
A nivel químico, el ácido láctico (INCI: Lactic Acid) es un ácido carboxílico, con un grupo hidroxilo en el carbono adyacente al grupo carboxilo, lo que lo convierte en un ácido α-hidroxílico (AHA) de fórmula H3C-CH(OH)-COOH, y con fórmula molecular C3H6O3. En solución acuosa puede perder el hidrógeno unido al grupo carboxilo y convertirse en el anión lactato, que a nivel biológico participa en diferentes procesos bioquímicos. Podemos encontrar en el mercado diferentes productos activos que incluyen esta forma lactato, como por ejemplo el Sodium Lactate o Potassium Lactate. Ambos destacan por sus propiedades hidratantes ya que son componentes que podemos encontrar de forma natural en la piel.
Ya hablamos de los AHA en una entrada del blog. A modo de apunte, recordamos que los AHA funcionan como exfoliantes químicos, ya que reducen la cohesión intercorneocitaria e interfieren con el enlace iónico intercelular. Esto provoca una aceleración del recambio celular en el estrato corneo. Los AHA son más efectivos promoviendo la renovación celular en la forma no ionizada, es decir, en su forma ácida. El recambio celular máximo se obtiene a pH 3. Por lo tanto, los productos que contienen AHA deberían de tener un pH lo más próximo posible a este valor. En la práctica no puede ser así, y lo veremos en el apartado de legislación ya que existen ciertas limitaciones a nivel de uso.
En comparación con el ácido acético , el pKa del ácido láctico es 1 unidad menor, lo que significa que el ácido láctico se desprotoniza diez veces más fácilmente que el ácido acético. Esta mayor acidez es la consecuencia del enlace de hidrógeno intramolecular entre el α-hidroxilo y el grupo carboxilato. El ácido láctico es un compuesto quiral, es decir, consta de dos isómeros ópticos . Uno se conoce como ácido L – láctico o ( S ) – ácido láctico y el otro, su imagen especular, es ácido D-láctico o ( R ) – ácido láctico . Una mezcla de los dos en cantidades iguales se llama ácido DL – láctico o ácido láctico racémico .
El ácido láctico es un compuesto sólido, de color blanco y que se puede comercializar como un polvo cristalino. Es totalmente soluble en agua, dando como resultado una solución totalmente transparente. Las soluciones que se encuentran en el mercado son habitualmente del 90-95%.
Para obtener ácido láctico a nivel industrial, se hace a través de un proceso de fermentación dónde se parte de carbohidratos simples como la glucosa, la sacarosa o la galactosa. Mediante cultivos bacterianos, estos sustratos se transforman en ácido láctico.
A la hora de formular un producto cosmético natural utilizando ácido láctico, tenemos que tener en cuenta si lo vamos a utilizar como agente estabilizador de pH, humectante o acondicionador. En estos casos caso se utilizará a dosis inferiores de hasta el 0,5% aproximadamente. Como AHA en formulaciones exfoliantes las dosis de uso pueden superiores, de hasta el 2.5%.
A pesar del uso generalizado del ácido láctico en cosmética natural, existe preocupación por la seguridad de los alfa hidroxiácidos. Debido a su potencial de irritación, la FDA se posicionó en el año 2000 ante el Comité Científico de Productos Cosméticos (SCCNFP) para que emitiera su opinión sobre el uso de los AHA.
Se consideró que era necesario realizar estudios de evaluación que contemplaran: la seguridad para el uso a largo plazo, la investigación del mantenimiento de la integridad de la función barrera de la piel (incluyendo los efectos sobre la absorción de otros ingredientes cosméticos), y la evaluación de los efectos de los AHA en las respuestas de la piel a la exposición a los rayos UV (estudios de foto-toxicidad). En 2004 se recopilaron algunos de los estudios llevados a cabo al respecto. No se pudo concluir el efecto de una forma concreta. Ante dicha situación, y atendiendo al principio de precaución se estimó que el ácido láctico se podía utilizar a una concentración máxima del 2.5% y un pH ≥ 5.
Además, se propuso la siguiente recomendación para los consumidores:

Para saber más sobre ingredientes cosméticos, en nuestra escuela puedes encontrar diferentes cursos dónde podrás aprender más sobre ingredientes y otros temas relacionados con la formulación cosmética.
1. CosIng – Cosmetics – GROWTH – European Commission [Internet]. [consultado 11 agosto 2020]. Disponible en: https://ec.europa.eu/growth/tools-databases/cosing/index.cfm?fuseaction=search.details_v2&id=34809
2. Ácido láctico – Chemistry LibreTexts [Internet]. [consultado 11 agosto 2020]. Disponible: https://chem.libretexts.org/Under_Construction/Walker/Chemicals/Substance%3AJKL/Lactic_acid1
3. The safety of alpha-Hydroxy acids. The scientific committee on cosmetic products and non-food products intended for consumers. position paper concerning the safety of alpha-hydroxy acids. 2000. Disponible: https://ec.europa.eu/health/ph_risk/committees/sccp/documents/out121_en.pdf
4. Nakagawa N, Sakai S, Matsumoto M, Yamada K, Nagano M, Yuki T, et al. Relationship between NMF (lactate and potassium) content and the physical properties of the stratum corneum in healthy subjects. J Invest Dermatol [Internet]. 2004 [consultado 11 de agosto 2020];122(3):755–63. Disponible en: https://pubmed.ncbi.nlm.nih.gov/15086563/
5. The scientific committee on cosmetic products and non-food products intended for consumers consumer safety of alpha-hydroxy acids. 2004. Disponible en: https://ec.europa.eu/health/ph_risk/committees/sccp/documents/out284_en.pdf
Escrito por María Cerdán.





Compras 100% seguras con:
![]()

Compras 100% seguras con:
![]()
¿Tienes alguna duda? Te llamamos gratis y sin compromiso. Déjanos tu teléfono y nos podremos en contacto contigo a la mayor brevedad.
Nuestro horario de atención es de 9:00 a 15:30 CEST